
Tất cả nội dung của iLive đều được xem xét về mặt y tế hoặc được kiểm tra thực tế để đảm bảo độ chính xác thực tế nhất có thể.
Chúng tôi có các hướng dẫn tìm nguồn cung ứng nghiêm ngặt và chỉ liên kết đến các trang web truyền thông có uy tín, các tổ chức nghiên cứu học thuật và, bất cứ khi nào có thể, các nghiên cứu đã được xem xét về mặt y tế. Lưu ý rằng các số trong ngoặc đơn ([1], [2], v.v.) là các liên kết có thể nhấp vào các nghiên cứu này.
Nếu bạn cảm thấy rằng bất kỳ nội dung nào của chúng tôi không chính xác, lỗi thời hoặc có thể nghi ngờ, vui lòng chọn nội dung đó và nhấn Ctrl + Enter.
Nghiên cứu mới liên kết nồng độ triglyceride cao với sự phát triển và vỡ phình động mạch chủ
Đánh giá lần cuối: 18.08.2025
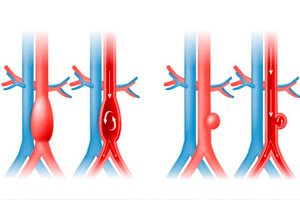 ">
">Một bài báo được công bố trên tạp chí Circulation đã kết hợp di truyền học con người và các mô hình thực nghiệm để đi đến một kết luận đơn giản: tăng triglyceride máu không chỉ là "người bạn đồng hành" của bệnh tim mạch mà còn là yếu tố chính gây phình động mạch chủ bụng (AAA). Ở chuột, nồng độ TG rất cao dẫn đến sự phát triển, bóc tách và thậm chí vỡ phình động mạch chủ nhanh hơn, trong khi nồng độ TG thấp (ASO xuống ANGPTL3) lại làm chậm quá trình tiến triển. Cơ chế là các axit béo (palmitate) "phá vỡ" quá trình trưởng thành của lysyl oxidase (LOX), một loại enzyme "liên kết chéo" elastin và collagen trong thành động mạch chủ; nếu không có LOX bình thường, mô sẽ trở nên lỏng lẻo và dễ bị tổn thương. Ở người, phân bố ngẫu nhiên theo Mendel đã xác nhận mối quan hệ nhân quả giữa lipoprotein giàu TG và nguy cơ phình động mạch chủ bụng (AAA).
Bối cảnh của nghiên cứu
Tại sao phình động mạch chủ bụng (AAA) là một vấn đề lâm sàng chưa được giải quyết?
Phình động mạch chủ bụng (AAA) là một tình trạng "im lặng" với tỷ lệ tử vong cao khi vỡ; hiện chưa có thuốc hiệu quả nào có thể làm chậm sự phát triển của nó một cách đáng tin cậy. Chiến lược hiện nay là sàng lọc siêu âm ở các nhóm nguy cơ và phẫu thuật khi đạt ngưỡng đường kính. Khuyến nghị của USPSTF: sàng lọc một lần ở nam giới từ 65-75 tuổi đã từng hút thuốc; ở phụ nữ không có yếu tố nguy cơ - không khuyến cáo.
Những phương pháp đã được thử nghiệm trước đây và tại sao chúng không hiệu quả
Một số phương pháp "chống phân hủy" (ví dụ, doxycycline như một chất ức chế metalloproteinase ma trận) đã không làm chậm được sự phát triển của AAA nhỏ trong RCT, làm giảm hy vọng về liệu pháp chống viêm/chống ma trận đơn giản.
Vai trò của lipid: trọng tâm chuyển sang các hạt giàu TG.
Trong khi LDL-C vẫn là yếu tố chính gây bệnh tim mạch vành, đối với AAA, ngày càng có nhiều dữ liệu chỉ ra lipoprotein giàu triglyceride (TRL, tàn dư). Các tổng quan hiện đại và nghiên cứu di truyền (bao gồm cả phân tích ngẫu nhiên Mendel) ủng hộ mối quan hệ nhân quả giữa TG/TRL tăng cao và nguy cơ AAA. Một bài báo mới trên Circulation (2025) đã kết hợp các phân tích MR và thí nghiệm và đi đến kết luận tương tự.
Cơ học thành mạch: nơi nó “tinh tế”
Sức mạnh của động mạch chủ được xác định bởi các “liên kết chéo” của collagen và elastin, do lysyl oxidase (LOX) đảm nhiệm. Họ LOX giúp ổn định ma trận ngoại bào; khi thiếu hụt/ức chế, động mạch chủ trở nên lỏng lẻo và dễ bị giãn nở - điều này đã được xác nhận bởi cả các bài đánh giá và mô hình thực nghiệm.
Tại sao ANGPTL3 là một mục tiêu hấp dẫn?
ANGPTL3 ức chế lipoprotein lipase; việc ức chế nó làm giảm đáng kể TG (và một phần các lipid khác). Đã có một loại thuốc chống ANGPTL3 được phê duyệt (evinacumab) và các phương pháp tiếp cận RNA đang được phát triển - tức là, đã có "công cụ" để thử nghiệm lâm sàng giả thuyết "giảm TG → ức chế AAA".
Tóm tắt bối cảnh
Lĩnh vực này đang chuyển dịch từ các ý tưởng chống viêm “phổ quát” sang trục lipid-ma trận: TRL/TG → phá vỡ sự trưởng thành của ma trận và “liên kết chéo” (bao gồm cả thông qua LOX) → làm suy yếu thành động mạch chủ → phát triển/vỡ AAA. Trong bối cảnh này, nghiên cứu trên Circulation đã kiểm tra một cách logic mối quan hệ nhân quả với di truyền học và cho thấy trong các mô hình rằng việc điều chỉnh TG có thể làm chậm tiến triển - đây là cầu nối giữa dịch tễ học và cơ chế còn thiếu để khởi động các thử nghiệm lâm sàng.
Họ thực sự đã làm gì?
- Con người (di truyền): áp dụng phương pháp ngẫu nhiên Mendel, kết hợp dữ liệu về bộ gen, protein và chuyển hóa - và thu được tín hiệu nhân quả: lipoprotein giàu TG và protein/chất chuyển hóa liên quan đến chuyển hóa TG càng cao thì nguy cơ mắc AAA càng cao.
- Cơ chế (tế bào/mô): TG và palmitate tăng cao đã được chứng minh là làm gián đoạn quá trình trưởng thành của LOX và làm giảm hoạt động của nó → thành động mạch chủ mất đi các “liên kết chéo”, giãn nở và dễ rách hơn. Sự biểu hiện quá mức LOX tại chỗ trong động mạch chủ đã loại bỏ “tác hại” của chứng tăng triglyceride máu.
- Chuột (mô hình AAA):
- trong tình trạng thiếu hụt Lpl (tăng triglyceride máu cực độ), hầu hết các động vật trong mô hình angiotensin II đều chết do vỡ động mạch chủ;
- Apoa5-/- (TG vừa phải cao) - tăng trưởng nhanh của AAA;
- chuyển gen cho APOC3 của con người (TG rất cao) - tách lớp và đứt gãy.
- Bằng chứng về khái niệm điều trị: oligonucleotide antisense đối với ANGPTL3 làm giảm đáng kể TG và ức chế sự tiến triển của AAA ở chuột APOC3 chuyển gen và ở Apoe-/-.
Tại sao điều này lại quan trọng?
Phình động mạch chủ bụng là một tình trạng âm thầm và nguy hiểm: vỡ động mạch chủ thường dẫn đến tử vong, và hầu như không có thuốc hiệu quả nào để làm chậm sự phát triển của AAA (nền tảng là theo dõi/sàng lọc và phẫu thuật khi đạt ngưỡng). Nghiên cứu mới lần đầu tiên được thực hiện nghiêm ngặt và đa tuyến tính (di truyền → cơ chế → mô hình) cho thấy lipoprotein giàu TG là mắt xích quan trọng trong cơ chế bệnh sinh, và việc giảm mục tiêu của chúng có thể trở thành một chiến lược điều trị bằng thuốc chống lại AAA.
Chi tiết cần chú ý
- LOX là một "điểm yếu" của thành động mạch chủ. Lysyl oxidase "liên kết chéo" các sợi elastin và collagen. Các tác giả đã chỉ ra rằng palmitate cản trở quá trình trưởng thành của LOX, và đây là cầu nối trực tiếp từ quá trình chuyển hóa chất béo đến sức bền cơ học của động mạch chủ. Khi LOX được tăng cường nhân tạo tại vị trí phình động mạch, tác dụng chống phình động mạch đã trở lại, mặc dù TG cao.
- "Bằng chứng ngược": việc giảm TG về mặt dược lý (ANGPTL3-ASO) đã ức chế AAA trong hai mô hình độc lập, tăng cường khả năng hợp lý về mặt lâm sàng.
Điều này có ý nghĩa gì (có khả năng) đối với phòng khám?
- Mục tiêu mới - lipoprotein giàu TG. Nghiên cứu trong những năm gần đây đã chuyển trọng tâm của AAA từ "LDL nguyên chất" sang tình trạng viêm và tái cấu trúc ma trận. Ở đây, một liên kết TG cứng được thêm vào, với cơ chế rõ ràng thông qua LOX. Điều này mở ra không gian cho các thử nghiệm phòng ngừa/điều trị các tác nhân hạ TG - từ ức chế ANGPTL3 đến các con đường khác để điều chỉnh chuyển hóa TG.
- Các dấu ấn sinh học và phân tầng rủi ro: Nếu mối liên quan được xác nhận trong các nhóm đối chứng triển vọng, TG và mức độ hạt giàu TG có thể được đưa vào các thuật toán đánh giá rủi ro và lựa chọn để giám sát chặt chẽ hơn ở những bệnh nhân bị AAA nhỏ/trung bình.
Tuyên bố miễn trừ trách nhiệm quan trọng
- Chuột không phải là người: Hiệu quả điều trị của ANGPTL3-ASO và khả năng phục hồi LOX được chứng minh trên các mô hình tiền lâm sàng; chưa có dữ liệu lâm sàng. Cần có các thử nghiệm lâm sàng ngẫu nhiên có đối chứng (RCT) để kiểm tra xem việc giảm TG có làm chậm sự phát triển của AAA ở người hay không.
- MR - về quan hệ nhân quả, nhưng "trung bình". Phân tích ngẫu nhiên Mendel làm giảm các yếu tố gây nhiễu, nhưng cho thấy sự gia tăng TG được xác định về mặt di truyền suốt đời, chứ không phải những biến động ngắn hạn ở một bệnh nhân cụ thể. Việc chuyển sang can thiệp bằng thuốc đòi hỏi một xét nghiệm độc lập.
Bối cảnh: Tại sao khám phá này có ý nghĩa
Hình ảnh minh họa như sau: Lipoprotein giàu TG → axit béo (palmitate) → khiếm khuyết LOX → thành động mạch chủ yếu → phình/vỡ AAA. Trước đây, AAA có liên quan đến tình trạng viêm, thoái hóa ma trận và rối loạn chức năng cơ trơn; nghiên cứu mới này đặt thành phần lipid vào đúng trung tâm của các quá trình này - và cung cấp một "nút" can thiệp đã được kiểm chứng (hạ TG).
Nguồn: Liu Y. và cộng sự. Circulation (Xuất bản trước khi in, ngày 5 tháng 8 năm 2025): “Tăng triglyceride máu là yếu tố chính góp phần vào sự phát triển và vỡ phình động mạch chủ bụng: Thông tin chi tiết từ các mô hình di truyền và thực nghiệm.” https://doi.org/10.1161/CIRCULATIONAHA.125.0747
